CRISPR-Cas9 против анемии: генная терапия на пороге клиник
Итак, CRISPR выходит на финишную прямую к одобрению FDA. Но путь туда лежит через строжайший контроль: регуляторы и их независимые эксперты будут вглядываться в каждую цифру, задавать самые неудобные вопросы. Без этого никуда.
Итак, 31 октября внешние консультанты FDA начали то самое историческое обсуждение. Их цель — терапия для людей с серповидно-клеточной анемией. Что это за болезнь? Представьте, что идеально круглые, скользкие эритроциты — наши переносчики кислорода — вдруг становятся похожими на острые серпы. Они цепляются друг за друга, закупоривают сосуды, вызывая мучительные боли. Жизнь превращается в череду кризисов. А теперь представьте, что эту поломку в ДНК можно починить. Компании Vertex Pharmaceuticals и CRISPR Therapeutics утверждают, что их препарат exa-cel на это способен. Но прежде чем сказать «да», эксперты выверят на безопасность каждый его шаг.
«Ключевым моментом является безопасность», — не устает повторять Марк Уолтерс, педиатр из детской больницы в Окленде. И он знает, о чем говорит: Уолтерс консультировал разработчиков exa-cel. Его фраза — не формальность, а суровая реальность. Когда вмешиваешься в самый фундамент жизни, цена ошибки слишком высока.
Как работает эта генная магия? Разберем по полочкам
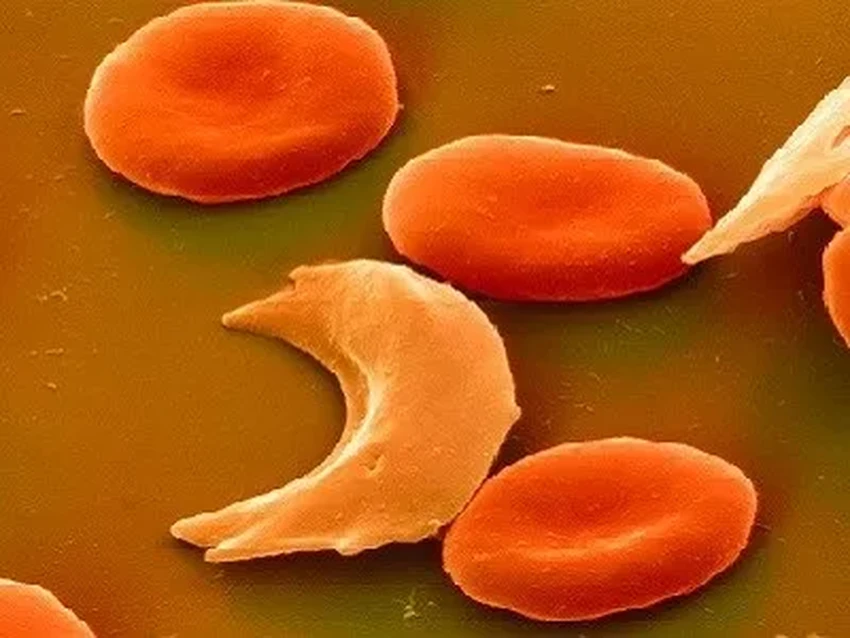
Вся беда в гемоглобине — том самом белке, что захватывает кислород. Из-за генетической ошибки он строится неправильно, деформируя эритроцит. Клетки слипаются в комки, сосуды забиваются, ткани задыхаются без кислорода. Отсюда и адские боли.
Exa-cel действует с хитроумным изяществом. Он не чинит сломанный ген напрямую. Вместо этого препарат «будит» спящего союзника — фетальный гемоглобин. Это особая форма белка, которая работает у нас только в утробе матери, а после рождения его производство глушит специальный ген-«выключатель» BCL11A. CRISPR-терапия приходит и ломает этот выключатель. Производство фетального гемоглобина возобновляется! И он, будучи здоровым, компенсирует работу дефектного. Гениально, правда?
Результаты звучат как фантастика: спустя 9 месяцев после лечения у 31 из 32 участников испытаний не случилось ни одного болезненного криза. До терапии они переживали в среднем по четыре таких атаки в год. Это не просто улучшение — это возвращение к нормальной жизни.
Но где прорыв, там и тревога. Главный страх — рак
Тень уже падала. У двух пациентов, прошедших другую генную терапию от той же анемии (от компании Bluebird Bio), позже развился рак крови. Правда, расследование показало, что вирус-переносчик здесь был не виноват. Но осадок остался.
Это заставило насторожиться: а что, если сам процесс «извлечения-редактирования-возвращения» стволовых клеток крови может спровоцировать рак? Есть данные, что люди с серповидно-клеточной болезнь и так более уязвимы к онкологии крови. А если среди взятых на редактирование клеток уже таилась предраковая? Не даст ли ей эта процедура рокового толчка к росту? «Это принципиальное, долгосрочное, потенциальное осложнение, с которым нам предстоит разобраться», — честно признаёт Уолтерс.
Разработчики это понимают. Vertex и CRISPR Therapeutics предлагают наблюдать за каждым пациентом 15 лет. Пятнадцать лет! Это не просто протокол, это долгосрочное обязательство. Сможем ли мы, как общество, нести такую ответственность за последствия вмешательства в природу? Вопрос риторический, но от этого не менее важный.